Kunskapsläget kan ha förändrats genom att det har kommit ny forskning eller systematiska översikter av relevans för den aktuella frågeställningen. Sammanställda resultat och ett kunskapsläge med starkt vetenskapligt stöd är dock ofta tillförlitliga över tid.
Välkommen att läsa mer i SBU:s Metodbok. Metodboken ger vägledning åt de som utför och granskar systematiska översikter inom hälso- och sjukvård, tandvården samt socialtjänst och funktionshinderområdet.
Molekylärdiagnostiska test för män med ökad sannolikhet för prostatacancer
Är du patient/anhörig? Har du frågor om egna eller anhörigas sjukdomar – kontakta din vårdgivare eller handläggare.
Sammanfattning och slutsatser
SBU:s bedömning av kunskapsläget
Många män låter på eget initiativ undersöka koncentrationen av prostataspecifikt antigen (PSA) i blodet. Hög PSA-koncentration tyder på ökad sannolikhet för cancer. Män med ökad sannolikhet utreds ofta vidare med vävnadsprovtagning från prostatakörteln (invasiv prostatabiopsi). Prostatabiopsi kan leda till komplikationer, och därför bör onödiga undersökningar undvikas. Lätt till måttligt förhöjd PSA-koncentration är ett svårtolkat resultat, och det är ofta oklart om biopsi är nödvändigt. För att undvika onödiga biopsier behövs nya, kompletterande test för att bättre avgöra vilka av de män som har lätt till måttligt förhöjd PSA-koncentration som behöver utredas vidare.
Denna rapport utvärderar den diagnostiska tillförlitligheten hos tre nya molekylära urintest: uPCA3, TMPRSS2:ERG samt me-GSTP1, när dessa används som tillägg till tidigare utfört PSA-test eller ändtarmsundersökning, vid utredning av prostatacancer. Rapporten belyser inte screening för prostatacancer eller nyttan av att behandla prostatacancer. Vi har inte heller utvärderat de nya testens eventuella betydelse för bedömning av hur allvarlig sjukdomen är, sjukdomsprognos eller val av behandling.
- För män med ökad sannolikhet för prostatacancer, enligt PSA-test eller ändtarmsundersökning, ökar den diagnostiska tillförlitligheten något då uPCA3-testet läggs till. Ju högre uPCA3-värde, desto högre är sannolikheten för cancer. Ett uPCA3-resultat över tröskelvärdet innebär en något stärkt misstanke om prostatacancer. För vissa, annars svårbedömda, patienter skulle testet därför kunna bidra till en tidigare biopsi och en tidigare diagnos. uPCA3-testet kan dock inte utesluta prostatacancer hos män med ökad sannolikhet för sjukdomen. Tillförlitligheten hos uPCA3-testet är lika oavsett om mannen tidigare har biopserats med negativt resultat eller aldrig tidigare har biopserats.
- Att lägga till uPCA3-testet för att avgöra vilka patienter som bör biopseras medför en högre totalkostnad än direkt prostatabiopsi av alla män med ökad sannolikhet för prostatacancer enligt PSA-prov eller ändtarmsundersökning.
- uPCA3-testets betydelse för vidare utredning samt påverkan på sjukdomsförlopp och död bör utvärderas i kliniska studier. För att kunna bedöma uPCA3-testets patientnytta i klinisk rutin behövs bättre kunskap om värdet av den extra information som testsvaret ger i relation till andra riskfaktorer, exempelvis PSA-koncentration, ålder, ändtarmsundersökning och resultat av tidigare biopsier.
- Det vetenskapliga underlaget räcker inte för att bedöma den diagnostiska tillförlitligheten av urintesten TMPRSS2:ERG och me-GSTP1. Fler studier behövs.
Metod och målgrupp
Prostatacancer är den vanligaste cancersjukdomen hos svenska män med över 10 000 nya fall per år. Av dem som får diagnosen dör ungefär var fjärde av sin sjukdom. En tidig diagnos av prostatacancer, i ett skede då sjukdomen varken ger symtom eller går att upptäcka vid kroppsundersökning, kan vara till nytta. Men, tidig diagnostik kommer emellertid också att medföra ett stort antal kirurgiska ingrepp utan nytta för patienten och med risk för negativa effekter.
Idag låter många män på eget initiativ undersöka sin sannolikhet för prostatacancer utan att de har någon egentlig misstanke om sjukdom. Detta kallas ibland för ”vild screening”. Mannens sannolikhet för prostatacancer uppskattas då med hjälp av bl a mätning av PSA-koncen-trationen i blodet och/eller ändtarmsundersökning. PSA-koncentrationen har ett samband med storleken på prostata och ökar vid prostatacancer. Men PSA-koncentrationen påverkas även av annat än cancer och PSA-testet ger därför osäkra besked, särskilt vid lätt till måttligt förhöjda nivåer. För män med PSA-koncentration i den så kallade ”gråzonen”, 3–10 nanogram per milliliter, baseras beslut om vidare utredning på ytterligare faktorer som ålder, förväntad livslängd, ärftlighet, etnicitet, eventuella symtom, resultat från ändtarmsundersökning, eventuella resultat från tidigare biopsier, kvoten av fritt och bundet PSA i blod samt förändring av PSA-koncentrationen över tid. Trots tillägg av dessa faktorer är det svårt att bedöma risken för många av dessa män. Det finns ett behov av att bättre kunna identifiera vilka som löper störst risk att utveckla kliniskt betydelsefull cancer och som därmed behöver utredas vidare med vävnadsprovtagning direkt från prostatakörteln (invasiv prostatabiopsi).
Referensmetoden för att diagnostisera prostatacancer är idag prostatabiopsi. Metoden har hög specificitet1, vilket betyder att undersökningen mycket sällan tyder på en tumör hos friska män. Undersökning av vävnadsprov från en prostatatumör ger även viss information om den eventuella sjukdomens svårighetsgrad och vägledning för hur den ska behandlas. Det är dock ofta oklart om den identifierade tumören kräver intensiv behandling med kirurgi eller strålning, som i sig medför risker och obehag, eller om den faktiskt är ofarlig. Prostatabiopsier har dessutom begränsad sensitivitet2 och det finns en risk att missa tumörer. Många upplever prostatabiopsier som obehagliga och smärtsamma. Ingreppet medför också en risk för komplikationer som blödning och infektion.
En särskilt intressant målgrupp för bättre testmetoder är de män som har förhöjd PSA-koncentration men där en eller flera biopsiomgångar inte kunnat påvisa någon tumör. Till följd av biopsimetodens risk att missa tumörer tillhör dessa män fortfarande riskgruppen för prostatacancer. Det är oklart hur man ska följa dessa män med PSA-test och ytterligare biopsier.
Sammantaget medför dagens frivilliga undersökning av prostatahälsan att många patienter utsätts för både prostatabiopsier och bortoperation av prostatakörteln till nytta endast för ett fåtal patienter. Det är önskvärt att undvika onödiga prostatabiopsier, och det behövs också bättre metoder för att identifiera vilka av de tumörer som faktiskt identifieras som kräver behandling.
Under senare år har det utvecklats flera molekylärgenetiska test för prostatacancer: urinanalys av genuttrycket för PCA3 och TMPRSS2:ERG samt för metyleringsgrad av GSTP1 (me-GSTP1). Mängden av dessa genprodukter i urin har i flera studier visats ha ett samband med sannolikheten för prostatacancer. Testen genomförs på urinprov som tas i samband med ändtarmsundersökning och är icke-invasiva, snabba och enkla för patienten. Provmaterialet måste hanteras enligt särskilda protokoll men analyserna sköts på centrallaboratorier. För analys av genuttrycket för PCA3 i urin har Gen-Probe utvecklat ett test med ett rekommenderat tröskelvärde på 35. Sannolikheten för prostatacancer anses dock som större ju högre testresultat som uppmäts. Övriga test finns ännu inte i kommersiellt bruk.
Förhoppningen är att dessa nya test ska kunna användas för att avgöra vilka av de patienter med lätt till måttligt förhöjd PSA-koncentration som har ett verkligt behov av prostatabiopsi eller förnyad biopsi.
Frågor
- Kan de nya molekylärdiagnostiska urintesten, uPCA3, TMPRSS2:ERG respektive me-GSTP1, identifiera de män med lätt till måttligt förhöjd PSA-koncentration i blod som behöver fortsatt utredning med prostata-biopsi?
- Tillför tillägg med uPCA3-test någon diagnostisk tillförlitlighet utöver PSA-blodprov hos män med ökad sannolikhet för prostatacancer?
- Vad kostar testen? Är de kostnadseffektiva?
Diagnostisk tillförlitlighet
Alla patienter som deltog i de studier som vi har granskat hade ökad sannolikhet för prostatacancer enligt PSA-blodprov eller ändtarmsundersökning. Referenstest har varit minst åtta mellannålsbiopsier av prostata. Majoriteten av de inkluderade studierna har använt ett kommersiellt test från Gen-Probe, med ett tröskelvärde för positivt3 eller negativt4 svar vid 35.
- uPCA3-testet har en sensitivitet på 57 procent (95% KI5, 54 till 59), jämfört med prostatabiopsi (måttligt starkt vetenskapligt underlag
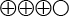 ). Det innebär att testet missade nästan hälften av de män där prostatacancer identifierades vid biopsi.
). Det innebär att testet missade nästan hälften av de män där prostatacancer identifierades vid biopsi. - uPCA3-testet har en specificitet på 74 procent (95% KI, 72 till 75) jämfört med prostatabiopsi (måttligt starkt vetenskapligt underlag
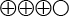 ). Det innebär att 74 procent av männen som inte uppvisade tumörer vid biopsi hade negativa PCA3-resultat.
). Det innebär att 74 procent av männen som inte uppvisade tumörer vid biopsi hade negativa PCA3-resultat. - I de studier som har inkluderats i denna översikt betyder ett positivt uPCA3-resultat att sannolikheten för sjukdom hade ökat från 31 till 50 procent (PPV6). Ett negativt uPCA3-resultat betydde att sannolikheten hade minskat från 31 till 21 procent (då NPV7 är 79 procent). Förändringen i sannolikhet för sjukdom mellan före och efter uPCA3-testet är liten, men kan ha viss betydelse vid ett positivt resultat.
- Enligt de inkluderade studierna har uPCA3-testet samma diagnostiska tillförlitlighet hos män som biopseras om efter tidigare negativ biopsi, som hos män som biopseras för första gången eller där gruppen är blandad.
- Vid en indirekt jämförelse mellan enbart PSA-testet och uPCA3-testet som tillägg till PSA-testet hade kombinationen något högre diagnostisk tillförlitlighet mätt som ytan under ROC-kurvan8. Resultatet gäller enbart män med ökad sannolikhet för prostatacancer enligt PSA-prov eller ändtarmsundersökning.
- Det vetenskapliga underlaget är otillräckligt (
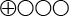 ) för att bedöma den diagnostiska tillförlitligheten av urintesten TMPRSS2:ERG och me-GSTP1.
) för att bedöma den diagnostiska tillförlitligheten av urintesten TMPRSS2:ERG och me-GSTP1.
Ekonomiska aspekter
- Det vetenskapliga underlaget är otillräckligt (
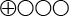 ) för att dra någon säker slutsats om uPCA3-testets kostnadseffektivitet.
) för att dra någon säker slutsats om uPCA3-testets kostnadseffektivitet.
I Sverige kostar ett uPCA3-test ungefär 85 procent av det som en omgång prostatabiopsier kostar. Tillägg av uPCA3-test för urval av vilka patienter som bör biopseras medför en högre totalkostnad än direkt prostatabiopsi av hela riskgruppen.
Fotnoter
1 Andelen friska som friskförklaras av testet.
2 Andelen sjuka som identifieras av testet.
3 Positivt testsvar indikerar sjukdom.
4 Negativt testsvar indikerar frånvaro av sjukdom.
6 Positivt prediktivt värde. Andelen av dem med positivt test som är sjuka.
7 Negativt prediktivt värde. Andelen av dem med negativt test som är friska.
8 ”Receiver operating characteristic”, en grafisk redovisning av testmetoders prestanda.
Gradering av styrkan i det vetenskapliga underlag som en slutsats grundas på görs i fyra nivåer:
Starkt vetenskapligt underlag (![]() ). Bygger på studier med hög eller medelhög kvalitet utan försvagande faktorer vid en samlad bedömning.
). Bygger på studier med hög eller medelhög kvalitet utan försvagande faktorer vid en samlad bedömning.
Måttligt starkt vetenskapligt underlag (![]() ). Bygger på studier med hög eller medelhög kvalitet med förekomst av enstaka försvagande faktorer vid en samlad bedömning.
). Bygger på studier med hög eller medelhög kvalitet med förekomst av enstaka försvagande faktorer vid en samlad bedömning.
Begränsat vetenskapligt underlag (![]() ). Bygger på studier med hög eller medelhög kvalitet med försvagande faktorer vid en samlad bedömning.
). Bygger på studier med hög eller medelhög kvalitet med försvagande faktorer vid en samlad bedömning.
Otillräckligt vetenskapligt underlag (![]() ). När vetenskapligt underlag saknas, tillgängliga studier har låg kvalitet eller där studier av likartad kvalitet är motsägande anges det vetenskapliga underlaget som otillräckligt.
). När vetenskapligt underlag saknas, tillgängliga studier har låg kvalitet eller där studier av likartad kvalitet är motsägande anges det vetenskapliga underlaget som otillräckligt.
SBU Alert bedrivs i samverkan med Läkemedelsverket, Socialstyrelsen och Sveriges Kommuner och Landsting.
Citera denna SBU Alert-rapport: SBU. Molekylärdiagnostiska test för män med ökad sannolikhet för prostatacancer. Stockholm: Statens beredning för medicinsk utvärdering (SBU); 2011. SBU Alert-rapport nr 2011-06. ISSN 1652-7151. http://www.sbu.se
Pressmeddelande
Urintest pusselbit när prostatacancer utreds
Urintester där man analyserar gener för att utreda prostatacancer är svårtolkade och kan inte användas för att utesluta cancer. Men vissa test kan vara ett komplement när läkaren bedömer vilka män som ska undersökas vidare.
Läs pressmeddelandetProjektgrupp
Sakkunniga
- Anders Bjartell, professor, överläkare, Skånes universitetssjukhus, Malmö
- Jan-Erik Damber, professor, överläkare, Sahlgrenska Universitetssjukhuset, Göteborg
SBU
- Susanna Kjellander, projektledare
- Ingegerd Mejàre, diagnostikresurs
- Anders Norlund, hälsoekonom
- Karin Rydin, biträdande projektledare och litteratursökare
- Lena Wallgren, projektassistent
Granskare
- Swen-Olof Andersson, docent, överläkare, Universitetssjukhuset, Örebro
- Ola Bratt, docent, överläkare, Helsingborgs lasarett, Helsingborg
- Elvar Theodorsson, professor, Universitetssjukhuset, Linköping

 Statens beredning för medicinsk och social utvärdering
Statens beredning för medicinsk och social utvärdering
 Dela sidan på Facebook
Dela sidan på Facebook
 Dela sidan på LinkedIn
Dela sidan på LinkedIn
 Dela sidan via E-post
Dela sidan via E-post